GLP-1RA在2型糖尿病治疗中的研究进展
原标题:Research progress of GLP-1RAs in the treatment of type 2 diabetes mellitus
5 分
关键词
摘要
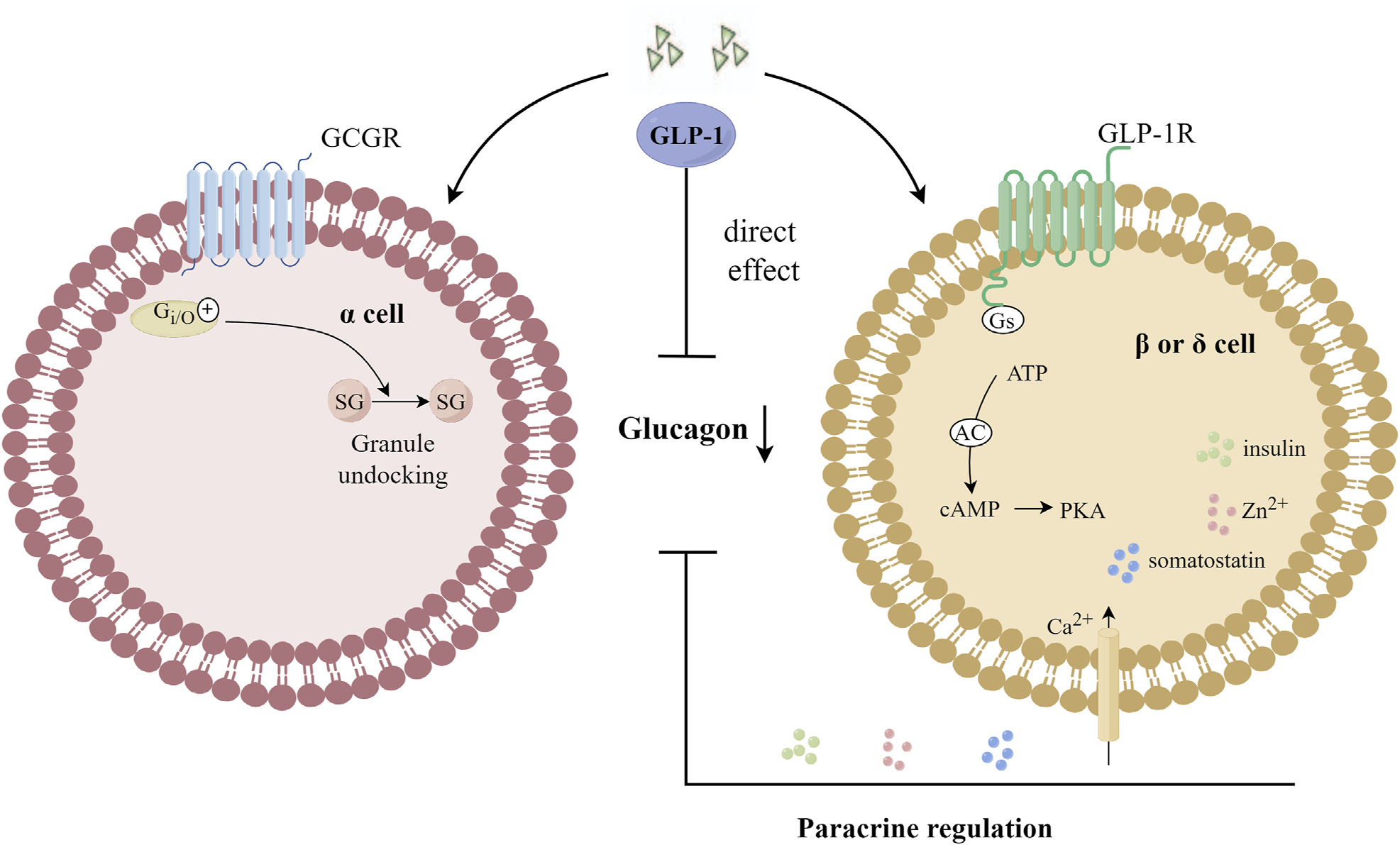
胰高血糖素样肽-1(GLP-1)是一种由30个氨基酸组成的肠道胰岛素刺激因子,主要由远端回肠和结肠的L细胞分泌。它具有多种生理功能,如促进胰岛素的分泌和合成、刺激β细胞增殖、诱导胰岛再生、抑制β细胞凋亡和胰高血糖素释放、延缓胃排空和控制食欲等。GLP-1通过分布在多个器官或组织中的特定GLP-1受体(GLP-1R)发挥作用,并参与体内葡萄糖稳态的调节。GLP-1受体激动剂(GLP-1RAs)具有与GLP-1相似的生理功能。由于其结构与天然GLP-1不同,不易被二肽基肽酶-4(DPP-4)降解,从而延长了作用时间。GLP-1RAs已被公认为一种新型降糖药,并广泛用于治疗2型糖尿病(T2DM)。与其他非胰岛素降糖药相比,它不仅能有效降低血糖和糖化血红蛋白(HbA1c),还可以保护心血管系统、神经系统和肾功能,而不会引起低血糖和体重增加。因此,GLP-1RAs具有良好的应用前景和进一步发展的潜力。
AI理解论文
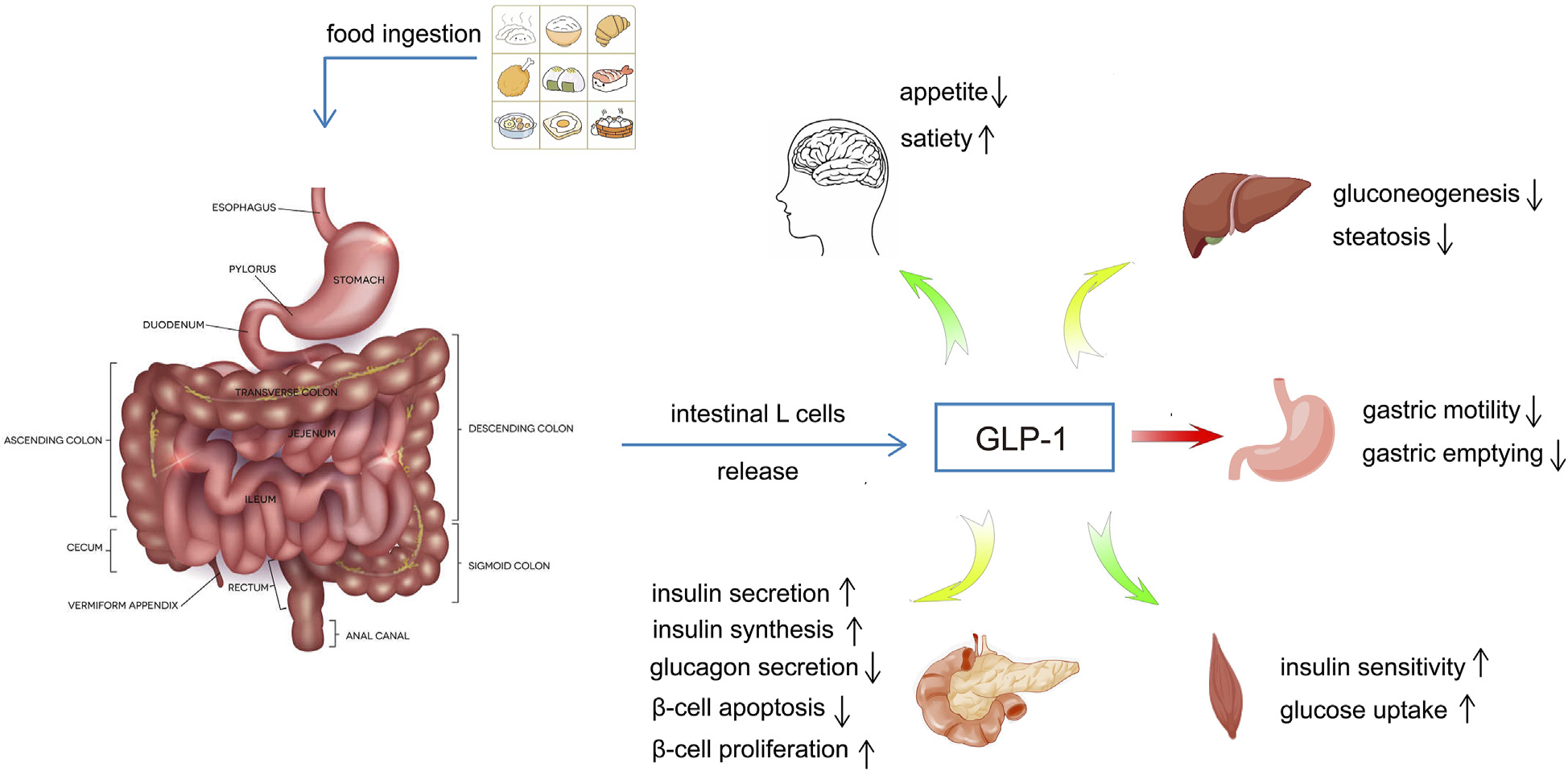


这篇论文主要探讨了GLP-1受体激动剂(GLP-1RAs)在2型糖尿病(T2DM)治疗中的研究进展。GLP-1是一种由肠道L细胞分泌的30个氨基酸组成的肠促胰岛素因子,具有促进胰岛素分泌和合成、刺激β细胞增殖、诱导胰岛再生、抑制β细胞凋亡和胰高血糖素释放、延缓胃排空和控制食欲等多种生理功能。GLP-1通过分布在多个器官或组织中的特定GLP-1受体(GLP-1R)发挥作用,参与体内葡萄糖稳态的调节。
GLP-1RAs的作用机制:GLP-1RAs模拟GLP-1的结构和功能,因其与天然GLP-1的结构差异,不易被二肽基肽酶-4(DPP-4)降解,从而延长了作用时间。GLP-1RAs被认为是一种新型的降糖药物,广泛应用于T2DM的治疗。与其他非胰岛素降糖药相比,GLP-1RAs不仅能有效降低血糖和糖化血红蛋白(HbA1c),还具有保护心血管系统、神经系统和肾功能的作用,并且不会引起低血糖和体重增加。
GLP-1分泌的影响因素:GLP-1的分泌主要受以下因素影响:1)相关受体的激活,如短链脂肪酸(SCFAs)激活的G蛋白偶联受体(GPCRs);2)肠道微生物群的结构组成;3)饮食因素,如高脂饮食会降低GLP-1分泌;4)Roux-en-Y胃旁路手术会显著增加餐后GLP-1和PYY浓度。
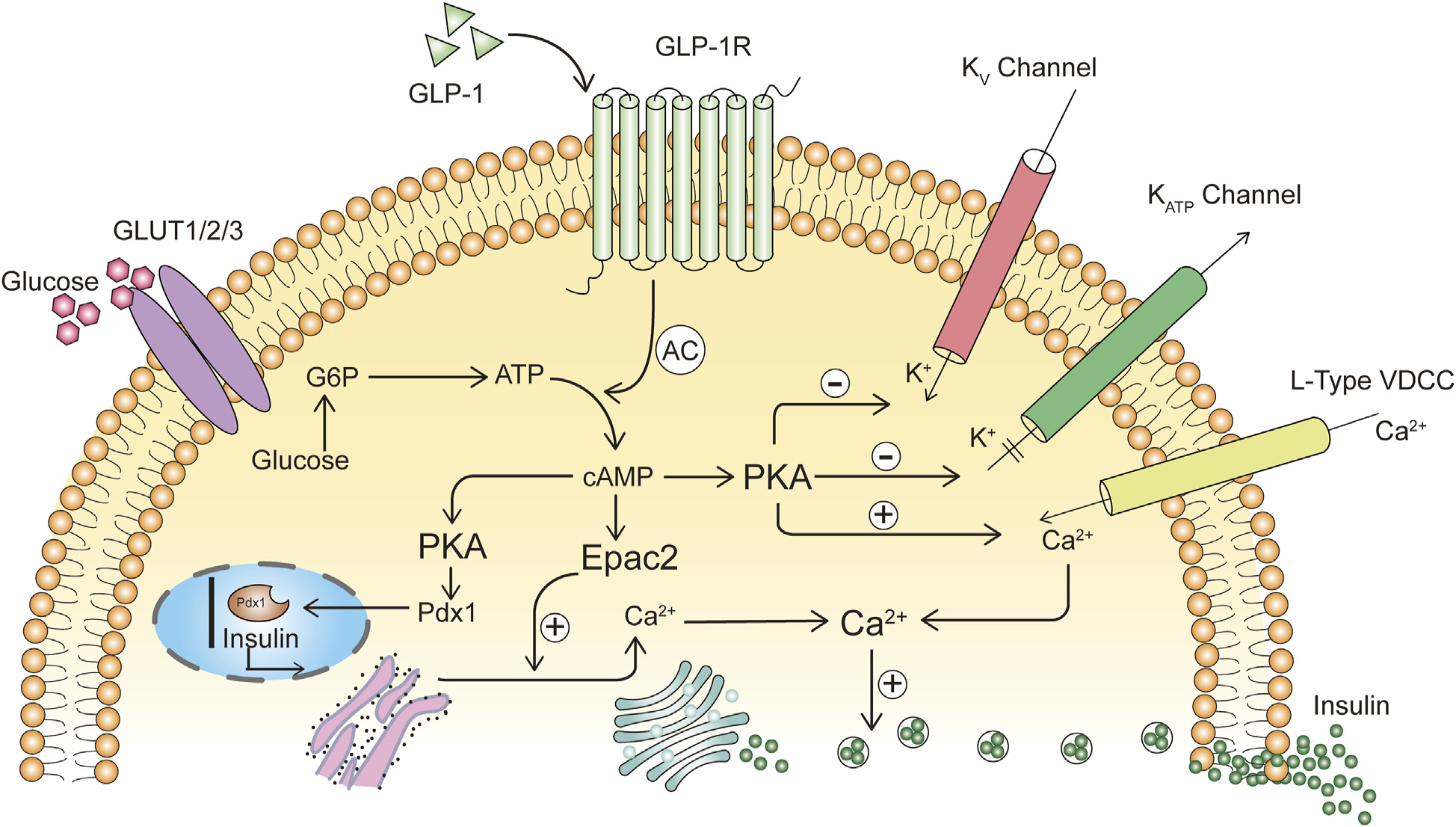
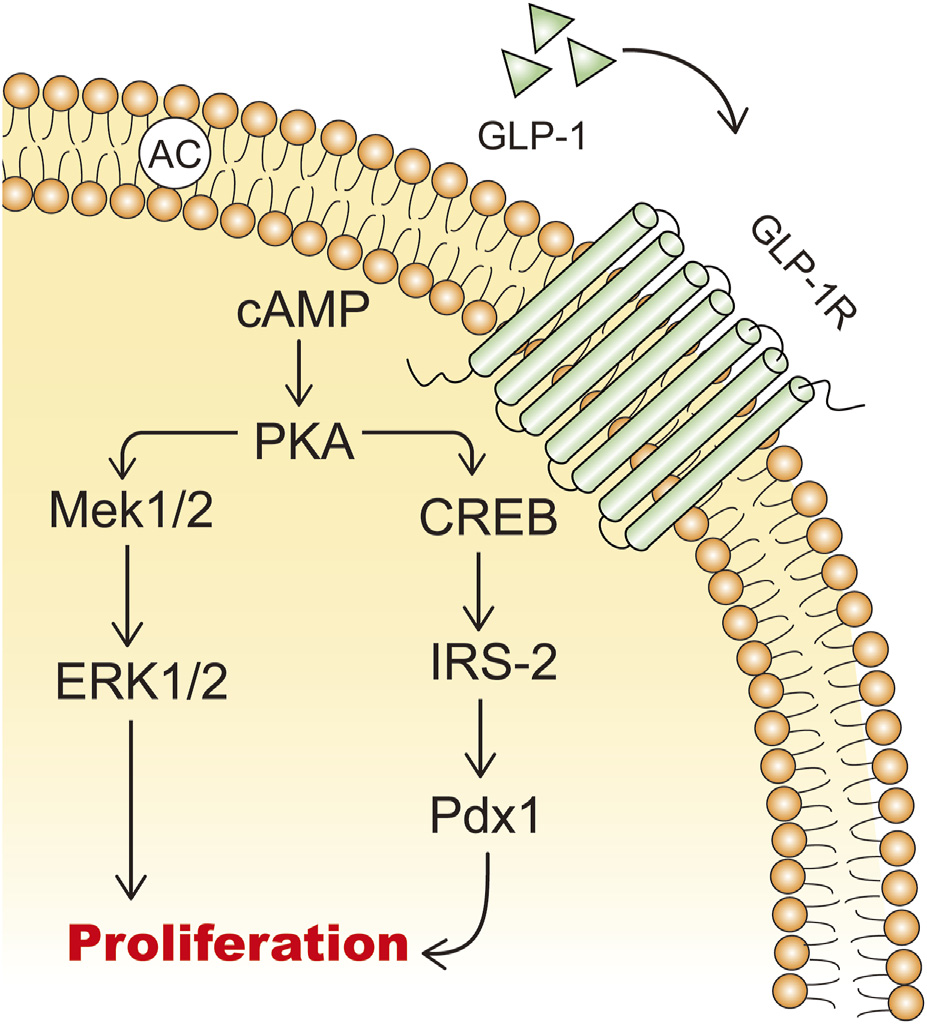
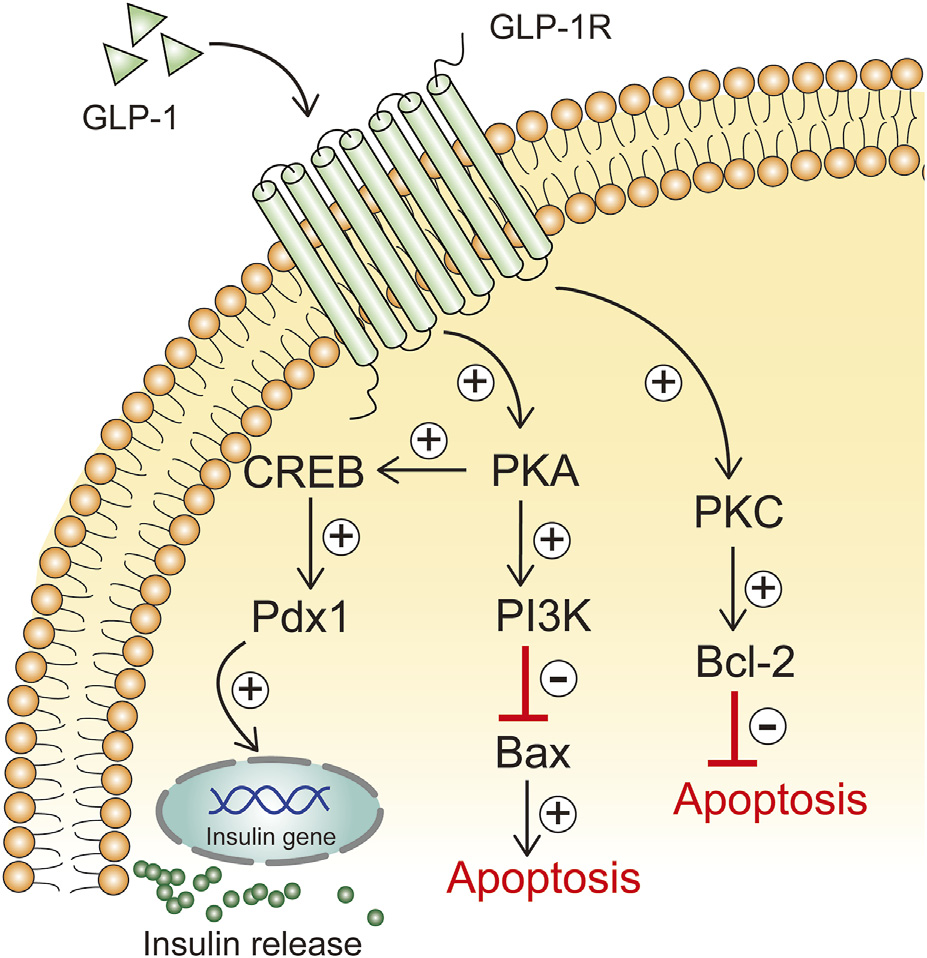
GLP-1调节血糖的机制和途径:GLP-1通过促进胰岛素合成和分泌来调节血糖。胰岛素合成的促进是通过GLP-1激活PKA,增加Pdx1的表达并使其转移到细胞核中,从而启动胰岛素基因的表达和合成。此外,GLP-1通过特定受体刺激胰岛β细胞的胰岛素分泌。
GLP-1RAs的临床应用:GLP-1RAs在临床上被广泛使用,其分类和用法在文中有详细的表格展示。GLP-1RAs不仅在血糖控制方面表现出色,还在体重管理、心血管保护和肾脏益处方面具有显著优势。
研究的贡献和意义:这篇综述文章的独特之处在于它深入探讨了GLP-1RAs在T2DM治疗中的多重机制,并比较了各种非胰岛素降糖药的作用特点、优缺点、注意事项和挑战。文章期望GLP-1RAs能够更安全、有效和合理地用于T2DM患者。
复杂术语解释:
- GLP-1(Glucagon-like peptide-1):一种肠促胰岛素因子,主要由肠道L细胞分泌。
- GLP-1RAs(GLP-1 receptor agonists):模拟GLP-1功能的药物,具有更长的半衰期。
- DPP-4(Dipeptidyl peptidase-4):一种酶,通常会降解GLP-1。
- SCFAs(Short chain fatty acids):短链脂肪酸,能激活特定的G蛋白偶联受体。
- Pdx1(Pancreatic/duodenal homeobox 1):一种关键的转录因子,参与胰腺发育和β细胞功能。
总之,这篇论文通过对GLP-1RAs在T2DM治疗中的作用机制、影响因素和临床应用的全面分析,为未来的研究和临床应用提供了重要的参考和指导。
