无监督无参考推断揭示了人类单细胞中未被识别的受调控转录组复杂性。
原标题:Unsupervised reference-free inference reveals unrecognized regulated transcriptomic complexity in human single cells
5 分
关键词
摘要
多种机制在DNA和RNA水平上多样化了真核生物转录本的序列内容,从而导致深远的功能后果。这种多样性的例子包括RNA剪接和V(D)J重组。目前,这些机制是通过零散的生物信息学工具检测的,这些工具需要预先定义一种转录本多样化的形式,并依赖于对不完整参考基因组的比对,过滤掉未比对的序列,这些序列可能对新的发现至关重要。在此,我们介绍了SPLASH+,显著推进了使用SPLASH进行生物学发现的可能性。SPLASH是我们最近推出的一种高效、无参考的统计方法。通过整合微组装和生物学解释框架,SPLASH+能够在单细胞中进行新的发现,包括广泛和新颖的转录本多样化例子,而无需细胞类型元数据,这是当前算法无法实现的。应用于使用SmartSeq2分析的来自19种组织的10,326个人类初级单细胞,SPLASH+发现了一组具有高度保守内含子区域的剪接和组蛋白调节因子,这些区域本身受到复杂的剪接调控。此外,它揭示了热休克蛋白HSP90AA1中未报道的转录本多样性,以及着丝粒RNA表达、V(D)J重组、RNA编辑和重复扩展中的多样化,这些都被现有方法忽略了。SPLASH+效率极高,通过一种新的自动化无偏转录组分析范式,使得在单细胞中发现前所未有的RNA调控和多样化成为可能。
AI理解论文
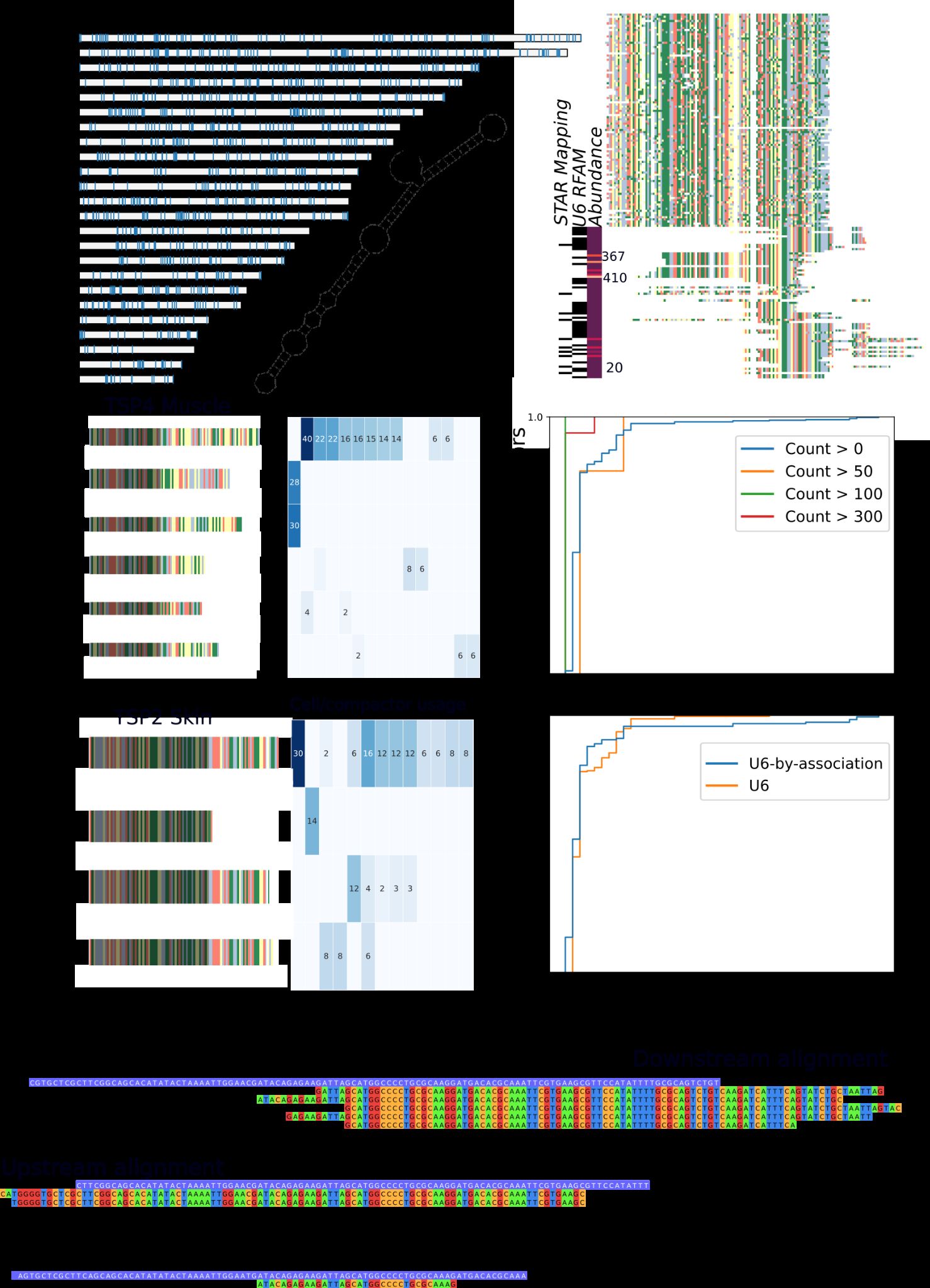



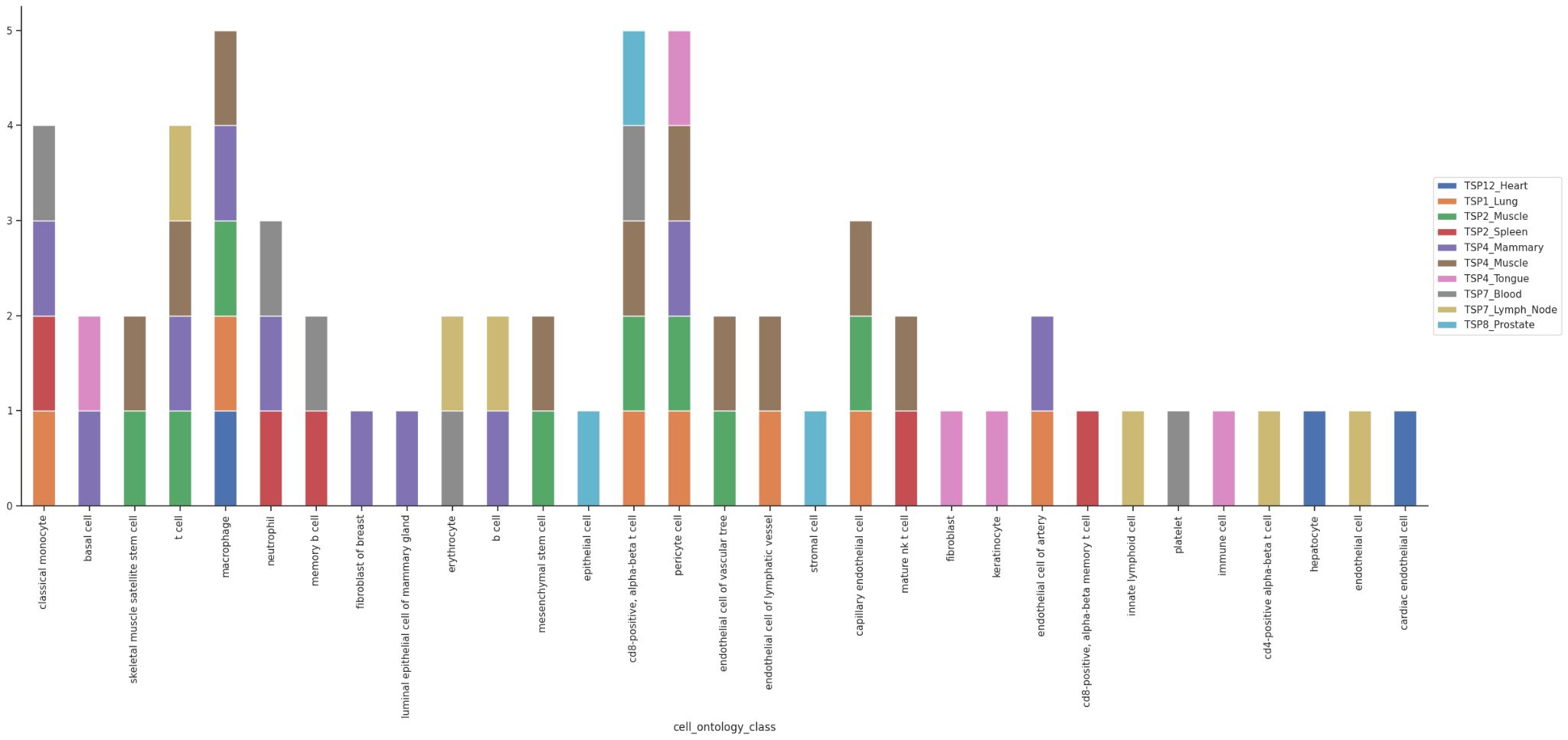


这篇论文介绍了一种名为NOMAD+的新分析方法,用于在单细胞水平上进行转录组多样性的无偏发现。论文的核心在于开发了一种统一的、无参考的统计推断方法,直接作用于原始测序读数,扩展了核心NOMAD算法,包含了微组装和解释框架。以下是论文的主要内容和贡献:
引言
在真核生物中,每个基因和非编码RNA位点可以通过多种机制产生多样的异构体,这些机制包括可变剪接、RNA编辑以及替代的5’和3’非翻译区(UTR)使用。这些机制可能导致功能上的显著差异,甚至与疾病有因果关系,如癌症和神经退行性疾病。尽管转录多样性对细胞特化的重要性,单细胞中这种多样性被调控的程度仍是基因组科学中的一个重要未解问题。
方法
NOMAD+方法通过跳过基因组比对,直接在原始测序读数上进行分析,避免了传统方法中由于依赖参考基因组而导致的盲点。传统的生物信息学工具通常需要预定义转录多样化的形式,并依赖于不完整的参考基因组,这会过滤掉未比对的序列,而这些序列可能是最有趣的。NOMAD+通过无监督的参考自由推断,揭示了人类单细胞中未被识别的转录组复杂性。
结果
在10,326个来自19种组织的初级人类单细胞中,NOMAD+发现了一组剪接和组蛋白调节因子,这些因子的内含子区域高度保守,并且是复杂剪接调控的目标。此外,还发现了热休克蛋白HSP90AA1中未报告的转录多样性。NOMAD+同时发现了着丝粒RNA表达的多样化、V(D)J重组、RNA编辑以及现有生物信息学方法无法测量的重复扩展。
讨论
NOMAD+是一种高效的统一算法,通过一种新的分析转录组的范式,实现了单细胞中RNA调控和多样化的无偏发现。该方法不仅适用于RNA-seq,还适用于DNA-seq研究,能够在大规模、统计驱动的转录组研究中发挥作用。NOMAD+的进一步发展和应用有望推动转录组学研究的进步,包括上游和下游的调控分析。
术语解释
- 可变剪接(Alternative Splicing):一种通过不同方式剪接RNA前体以产生多种mRNA异构体的过程。
- RNA编辑(RNA Editing):一种在RNA分子中通过化学修饰改变核苷酸序列的过程。
- V(D)J重组:一种在免疫系统中产生抗体多样性的基因重组过程。
- 非翻译区(UTR):mRNA中不被翻译成蛋白质的区域,参与调控基因表达。
结论
NOMAD+通过其无参考的分析方法,克服了传统生物信息学工具的局限性,提供了一种新的视角来研究单细胞中的转录组多样性。它不仅揭示了未被识别的转录组复杂性,还为未来的基因组和转录组分析提供了新的工具和方法。通过这种方法,研究人员可以更全面地理解转录组多样性及其在细胞功能和疾病中的作用。
