宽泛的过渡态集合是酶催化的重要组成部分
原标题:Wide transition-state ensemble as key component for enzyme catalysis
5 分
关键词
摘要
过渡态(TS)理论提供了理论框架,用以解释酶催化化学反应产生巨大速率加快的原因。鉴于蛋白质具有大量的构象集合,单一的过渡态将为酶催化构成一个巨大的熵瓶颈。为了解释这个问题,我们通过量子力学/分子力学计算研究了腺苷酸激酶中磷酰基转移步骤的酶促过渡态的性质。我们发现随着反应坐标而变化的结构上广泛多样的一组能量等价配置,因此存在一个广泛的过渡态集合(TSE)。包括不对称过渡态在内的构象离域的集合根植于酶的宏观特性。计算结果得到酶动力学实验的支持,这些实验证实了由于这种宽泛的TSE而预测的活化熵的降低。作为高效酶催化的关键,TSE进一步提升了一个统一的概念,即蛋白质折叠和构象转换是蛋白质功能的基础。
AI理解论文


这篇论文由Gabriel Ernesto Jara等人撰写,发表于2023年的eLife期刊,题为“Wide Transition-State Ensemble as Key Component for Enzyme Catalysis”。论文的核心在于探讨酶催化过程中过渡态的本质,特别是腺苷酸激酶(adenylate kinase)在磷酸转移步骤中的过渡态。研究结合了量子力学/分子力学(QM/MM)计算和实验验证,提出了一个**结构上宽泛的过渡态集合(Transition-State Ensemble, TSE)**的概念,并探讨其在酶催化中的重要性。
研究背景与动机
过渡态理论是理解酶催化反应速率加速的理论框架。传统观点认为,酶通过对过渡态的高亲和力来加速反应。然而,酶作为大分子,具有多种构象,这使得单一的过渡态可能成为酶催化的熵瓶颈。为了深入理解这一问题,研究者们选择了磷酸转移反应作为研究对象,因为这类反应在生物过程中普遍存在且未催化时能垒极高。
方法与技术
研究采用了量子力学/分子力学(QM/MM)模拟,这是一种结合量子力学和经典分子力学的方法,用于模拟复杂生物分子的反应过程。具体来说,研究使用了SCC-DFTB(Self-Consistent Charge Density-Functional Tight-Binding)方法进行模拟,并结合实验验证,包括温度和pH依赖的酶动力学研究,以及活性位点突变体的影响。
主要发现
-
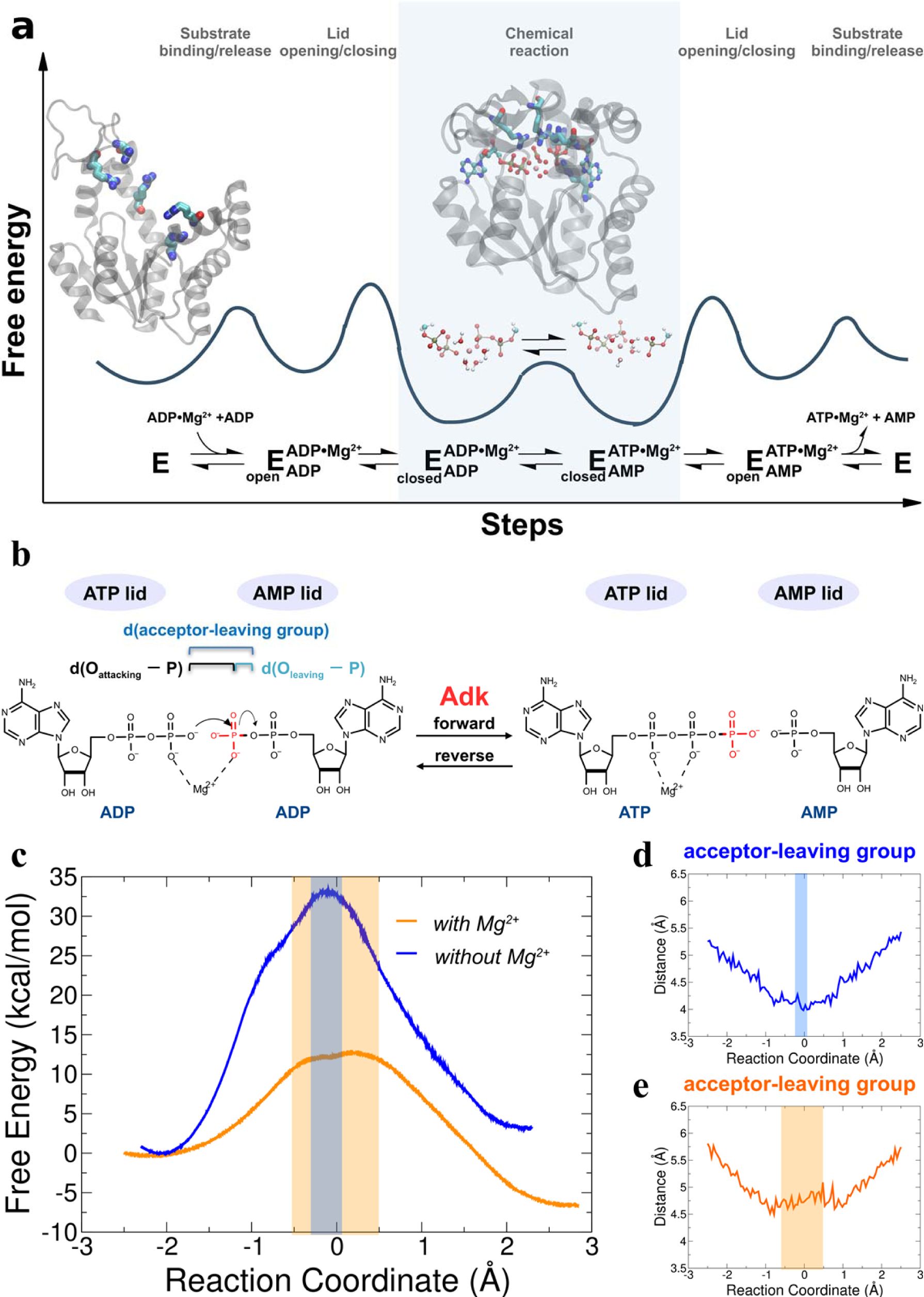
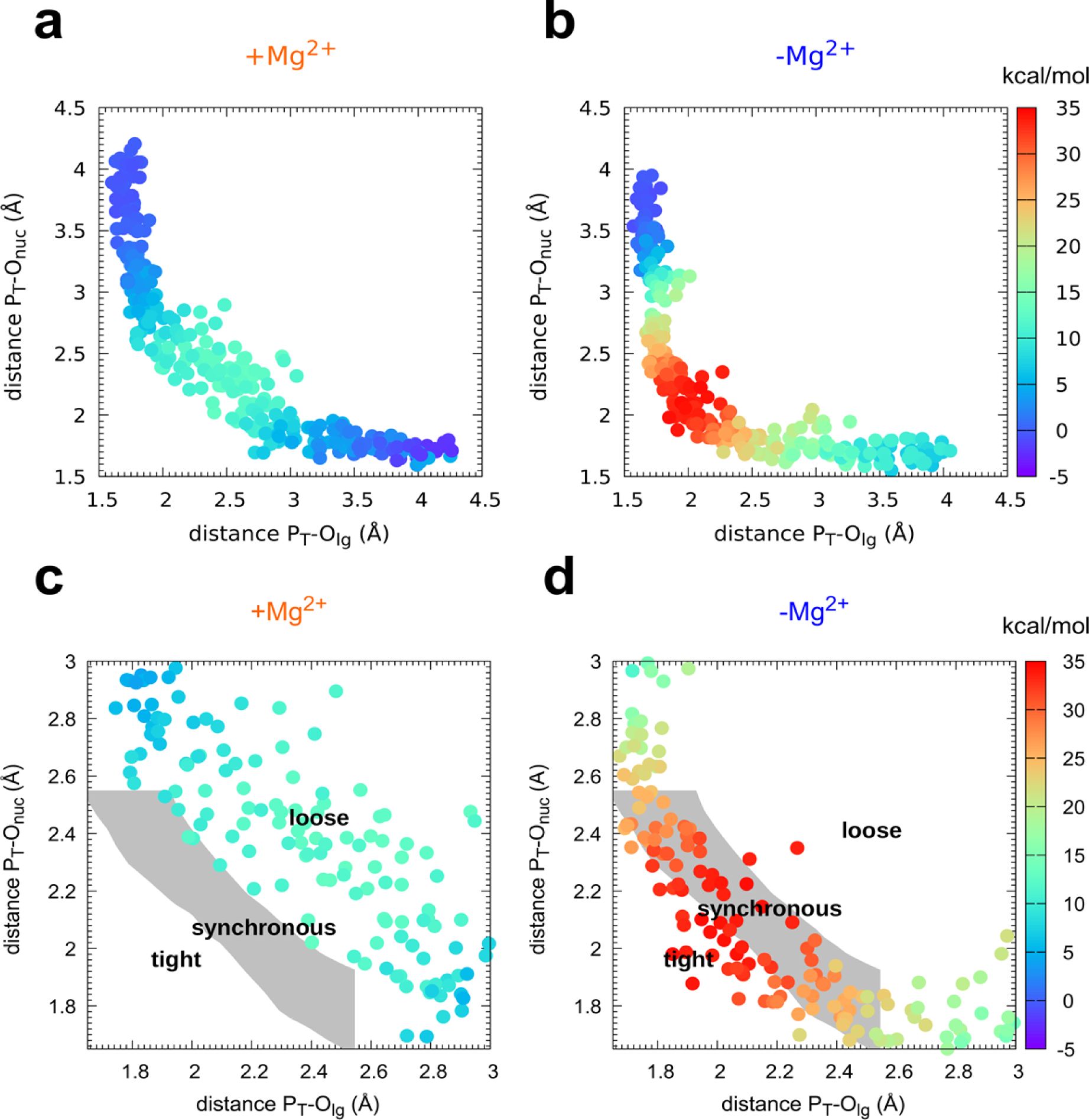
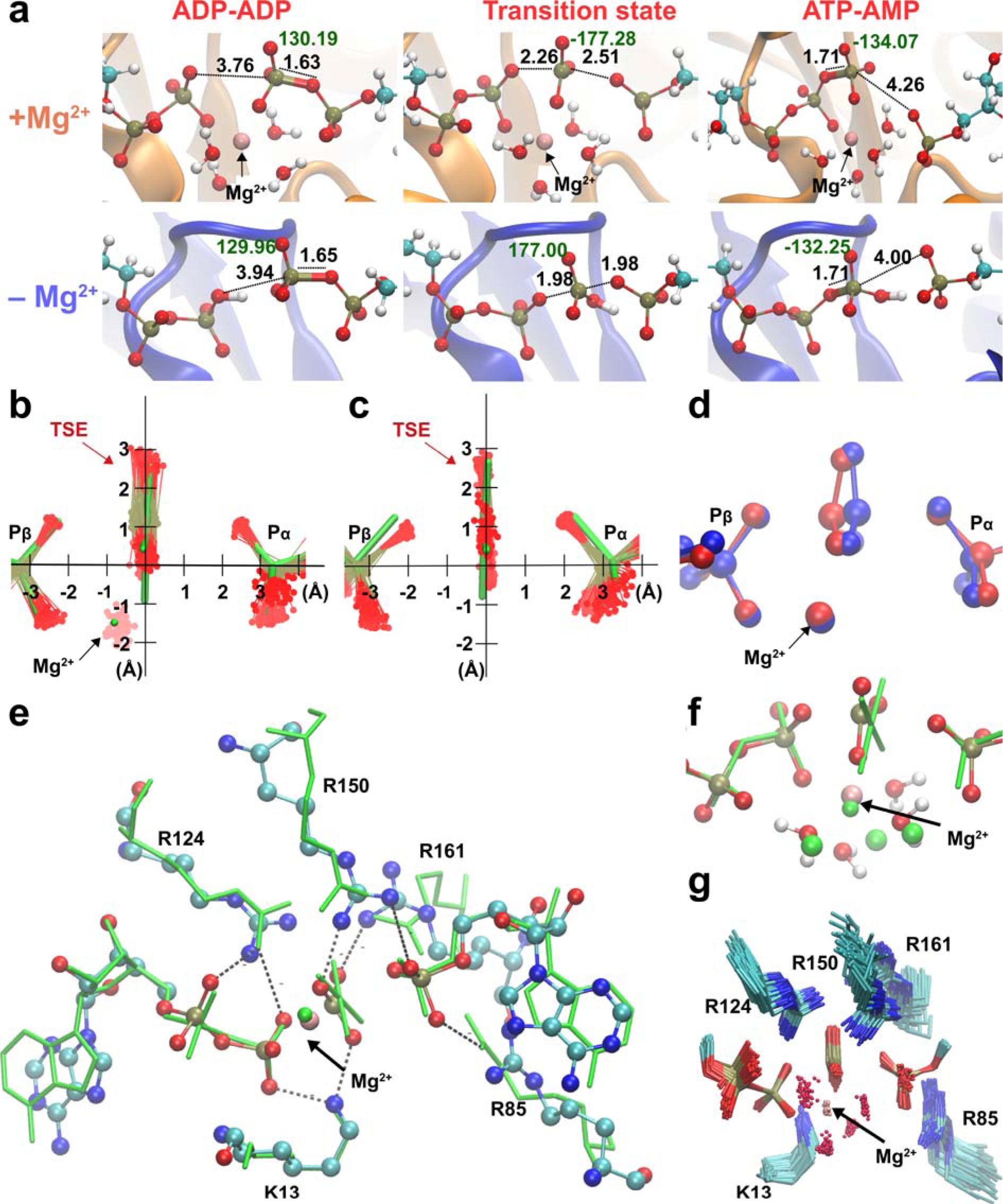
宽泛的过渡态集合:研究发现,腺苷酸激酶的磷酸转移步骤存在一个结构上宽泛的过渡态集合。这些过渡态在反应坐标上分布广泛,具有能量等价的多种构型。这种集合包括不对称的过渡态,表明酶的宏观性质导致了构象的分散。
-
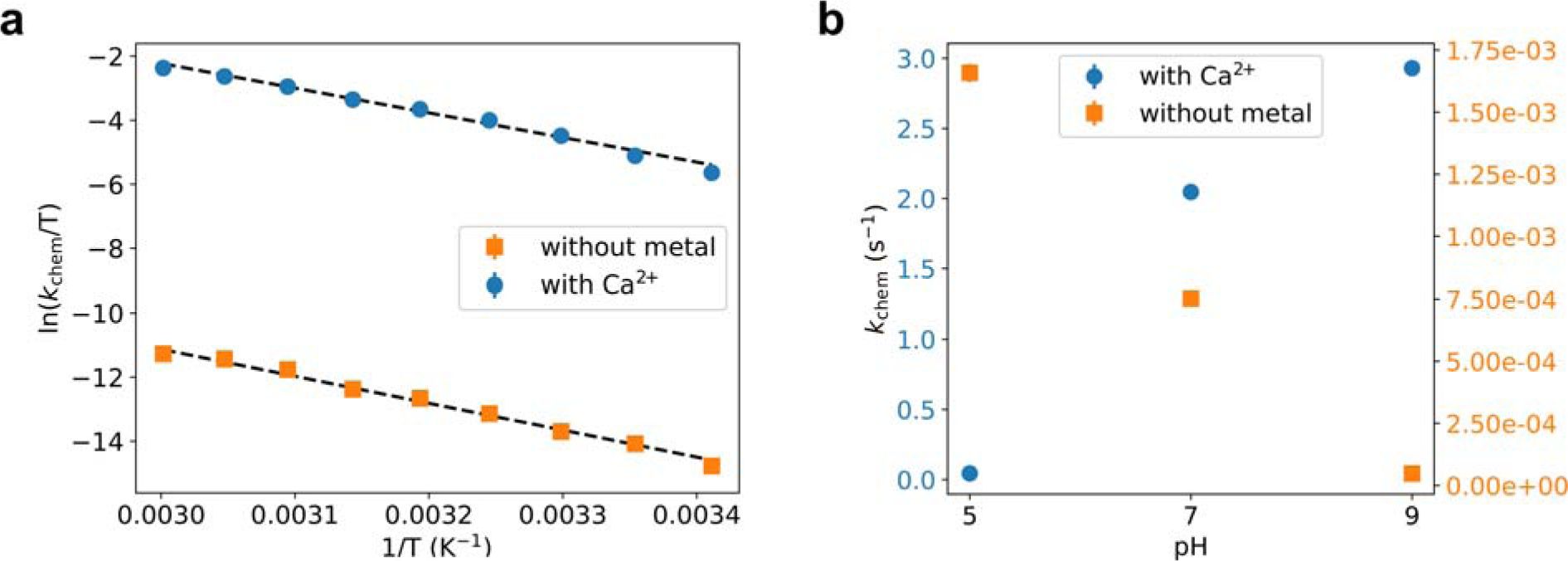
实验验证:通过酶动力学实验,研究验证了宽泛过渡态集合所预测的活化熵的降低。特别是,使用Ca2+离子代替Mg2+进行实验,观察到负的活化熵,这与模拟结果一致。
-
理论与实验的结合:研究通过QM/MM模拟和实验结果的结合,支持了过渡态集合在酶催化效率中的关键作用。这一发现为蛋白质折叠和构象转变提供了统一的概念框架。
讨论与意义
研究指出,传统的过渡态理论强调单一的过渡态,而该研究提出的宽泛过渡态集合概念挑战了这一观点。通过展示过渡态的多样性和分布,研究为理解酶的高效催化提供了新的视角。这一概念可能适用于其他酶系统,具有广泛的应用潜力。
研究的局限性与未来方向
尽管研究提供了重要的见解,但在过渡态集合的定义和实验结果的解释上仍存在一些不确定性。特别是,过渡态集合的定义应基于承诺分布(committor distribution),而非简单的能量范围。此外,实验结果与模拟之间的联系需要进一步的验证和探讨。
结论
这项研究通过整合QM/MM模拟和实验验证,揭示了酶催化过程中过渡态的复杂性和多样性。提出的宽泛过渡态集合概念为理解酶的高效催化提供了新的理论框架,并可能对未来的酶设计和生物催化研究产生深远影响。
